Проверка на бактериальные эндотоксины препаратов гиалуроновой кислоты.
21.03.2023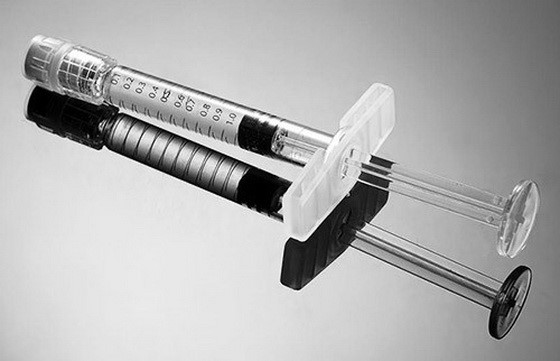
Демидова В.В. – Руководитель Испытательной лаборатории ООО «НПО «ЛАЛ-Центр»
Ожерельева А.С. – Руководитель организационного отдела Испытательной лаборатории ООО «НПО «ЛАЛ-Центр»
Гиалуроновая кислота является неотъемлемым компонентом многих сред и тканей организма [1] и обладает уникальными биохимическими и физическими свойствами, которые делают ее важным биоматериалом для применения в медицинских изделиях (МИ). Препараты гиалуроновой кислоты обладают широким спектром применения в медицинской практике и используются для лечения суставов при остеоартрите, остеоартрите и коксартрозе [2, 3], в хирургии глаза при установке интраокулярных линз [4] и при проведении коррекции окружающих тканей глаза (окулопластике) [5], в стоматологии для восстановления мягких тканей пародонта [6, 7], в общей хирургии в качестве противоспаечного барьера в брюшной полости [8], а также широкое применение нашли препараты гиалуроновой кислоты в косметологии – в настоящее время на фармацевтическом рынке насчитывается огромное разнообразие филлеров (косметических кожных наполнителей) для решения задач по улучшению эстетического и физиологического состояния кожных покровов.
Препараты гиалуроновой кислоты обычно классифицируются как медицинские изделия, а поскольку они представляют собой жидкие формы, которые вводятся пациенту инъекционно, они в обязательном порядке должны проходить контроль на содержание бактериальных эндотоксинов. Требования к жидким МИ в части содержания бактериальных эндотоксинов практически такие же, как и для лекарственных препаратов. Предельное содержание рассчитывается исходя из способов введения и доз конкретного препарата гиалуроновой кислоты.
Для наиболее распространенных препаратов – кожных наполнителей или филлеров, нормы содержания бактериальных эндотоксинов могут находится в ряду значений:
-
<0,07 ЕЭ/мг, монография «Натрия гиалуронат для инъекций» из фармакопеи USP;
-
<0,5 ЕЭ/мг или <0,05 ЕЭ/мг, монография «Натрия гиалуронат» из European Pharmacopoeia 8.0, для парентерального и внутриглазного/внутрисуставного введения соответственно;
-
<0,5 ЕЭ/мг, ФС «Натрия гиалуронат, раствор для внутрисуставного введения» ГФ РФ действующего издания;
-
<0,6 ЕЭ/мг, НД на препараты натрия гиалуроната серии «Repart».
Препараты гиалуроновой кислоты получают из тканей животных или путем микробиологического синтеза, а следовательно, препараты могут быть загрязнены бактериальными эндотоксинами. Проверка на эндотоксины готовых медицинских изделий на основе гиалуроновой кислоты осложняется высокой вязкостью этих препаратов. Так 2% - 2,5% препараты-филеры в шприцах очень вязкие и с трудом дозируются.
|
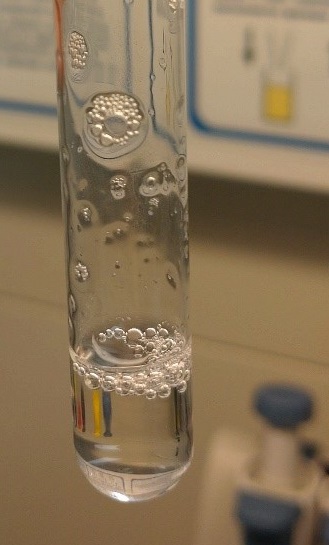
Рис. 1. Дозирование препарата гиалуроновой кислоты. |
|
|
|
Из шприца препарат выходит в виде густой, вязкой, труднорастворимой капли |
Для анализа же препараты, как правило, должны быть разведены в 50 – 100 раз на воде для ЛАЛ-теста. Первичное растворение, до 1/10, проходит трудно и часто приходится прибегать к нагреванию, длительному перемешиванию, ультразвуковой обработке. Начиная с разведения 1/100 получаемый раствор прозрачен и легко дозируется. В действительности добиться получения приемлемого для проведения анализа раствора препаратов гиалуроновой кислоты можно, но пробоподготовка осложнена именно высокой вязкостью препарата, что может приводить к ошибкам дозирования, к тому же, нельзя исключить, что бактериальные эндотоксины могут связываться с высокомолекулярными полимерами гиалуроновой кислоты и, в этом случае, в анализе возможна регистрация более низких, чем реальные, уровней содержания эндотоксина, особенно при высокой вязкости исходного препарата.
Возможным решением проблемы пробоподготовки высокомолекулярных вязких гелей гиалуроновой кислоты может стать использование на ранних этапах разведения фермента гиалуронидазы. Данный фермент, относящийся к классу эндогликозидаз, расщепляет гиалуроновую кислоту на моносахариды (до глюкозамина и глюкуроновой кислоты). Ферментативное расщепление гиалуроновой кислоты может упростить сам процесс подготовки разведения вязкого раствора. Возможно, что расщепление высокомолекулярных полимеров гиалуроновой кислоты может облегчить регистрацию эндотоксинов. Мы решили использовать ферментативную деградацию гиалуроновой кислоты на самых первых этапах разведения вязкого геля.
Препараты гиалуронидазы выпускаются в том числе и в качестве готовых лекарственных средств (чаще под названием «лидаза») и поэтому коммерчески доступны.
Содержание опыта
Нами выдвинуто предположение, что если перед разведением препарата гиалуроновой кислоты обработать ее расщепляющим ферментом, то это облегчит дальнейший процесс разведения, поможет избежать ошибок на стадии дозирования и, возможно, приведет к большему высвобождению эндотоксинов, если они присутствуют в проверяемом препарате.
В качестве препарата гиалуроновой кислоты был выбран готовый коммерческий препарат – Гель косметический на основе модифицированного гиалуроната натрия 2,4% в дозаторе. Расщепление проводили препаратом гиалуронидазы в виде готового коммерческого препарата – Лидаза 1280 МЕ (64 УЕ).
Первый шаг – разведение геля и получение из него менее вязкого раствора. Для этого готовили разведение 1/10 на воде для ЛАЛ-теста с добавлением гиалуронидазы. Вначале, добавили к 100 мкл препарата 800 мкл воды для ЛАЛ-теста, перемешали смесь в ультразвуковой ванне в течение часа при комнатной температуре. Первичные шаги разведения представлены на рис.2 и рис.3:
|
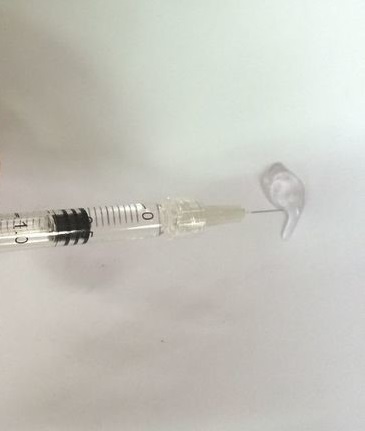
Рис.2. Дозирование из шприца |
|
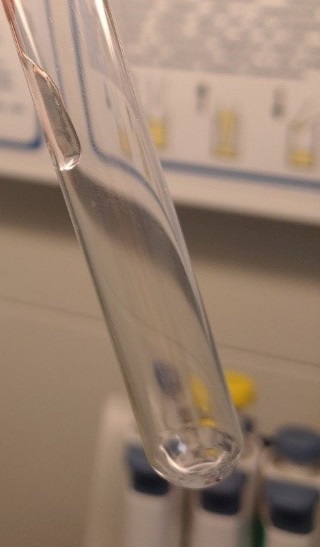
Рис. 3. Разведение водой для ЛАЛ-теста в отношении 1/9 |
|
|
|
|
|
Препарат очень вязкий, с трудом выдавливается из шприца в виде густой тягучей капли. |
|
Раствор слегка опалесцирующий, на стенках пробирки видны комки нерастворенного препарата. |
Далее к полученному вязкому раствору добавляли раствор гиалуронидазы 1280 МЕ/мл в количестве 100 мкл. В итоге получили разведение исходного препарата – 1/10. Раствор перемешивали на вихревой мешалке в течение часа при комнатной температуре.
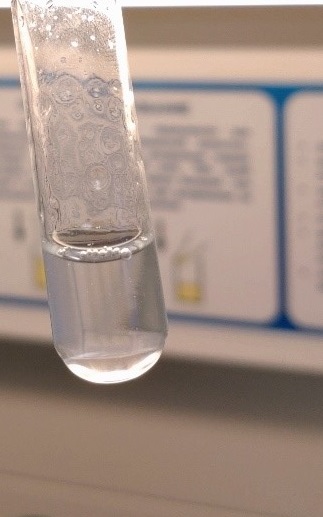
Эффект от воздействия фермента оказался заметным, полученный раствор был прозрачен и свободен от комков не растворившегося геля (рис.4).
|
Рис. 4. Раствор после обработки гиалуронидазой |
|
|
|
Получен прозрачный раствор, комки и сгустки отсутствуют |
Далее этот раствор разводили на воде для ЛАЛ-теста до конечной степени разведения исходного препарата гиалуроната натрия равного 1/100.
Параллельно готовили разведение исходного препарата гиалуроновой кислоты на воде для ЛАЛ-теста, также в отношении 1/100 с использованием стандартного трудоемкого набора операций пробоподготовки для уменьшения вязкости и достижения относительной однородности получаемого разведения: нагревание исходного геля, перемешивание водного разведения (не менее часа), обработка разведения в ультразвуковой ванне (не менее часа).
Полученные двумя разными способами испытуемые растворы препарата проверялись на содержание бактериальных эндотоксинов в ЛАЛ-тесте количественным кинетическим турбидиметрическим методом (методом С).
Результаты
Препарат «Гель косметический на основе модифицированного гиалуроната натрия 2,4% в дозаторе», поставленный в опыт содержал небольшое количество бактериальных эндотоксинов. Собственно, поэтому он и был выбран, нам хотелось увидеть есть ли разница в определяемой концентрации эндотоксинов при разной обработке исходного раствора. В испытуемом растворе, приготовленном с помощью фермента гиалуронидазы также были зарегистрированы бактериальные эндотоксины, причем в большей концентрации, чем в контрольном растворе.
Почему концентрация эндотоксинов в обработанном гиалуронидазой препарате оказалась больше чем в контроле? Возможны два объяснения:
-
Расщепление гиалуроновой кислоты под действием фермента, возможно, приводит к высвобождению эндотоксина, который в интактном препарате может быть связан с высокомолекулярным полимером гиалуроновой кислоты.
-
В использованном препарате гиалуронидазы также было фоновое содержание бактериальных эндотоксинов и в результате проделанных манипуляций мы получили кумулятивный эффект по эндотоксинам в испытуемом растворе. Результирующая концентрация эндотоксинов в обработанном гиалуронидазой испытуемом растворе оказалась выше, чем в испытуемом растворе, приготовленном только на воде для ЛАЛ-теста.
Заключение
Нашей задачей являлся поиск приемлемого способа проверки гелей на основе гиалуроновой кислоты, который помог бы решить вопрос высокой вязкости этих препаратов и сложности их разведения.
Опробованный нами вариант с использованием на ранней стадии разведения фермента гиалуронидазы, расщепляющей высокомолекулярный полимер гиалуроновой кислоты на моносахариды, может рассматриваться как перспективный вариант пробоподготовки.
Полученные результаты свидетельствуют о том, что обработка гиалуронидазой облегчает работу по разведению образца. Такая подготовка также не мешает определению бактериальных эндотоксинов в обработанном препарате. Не исключено, что обработка ферментом, расщепляющем молекулы гиалуроновой кислоты, может даже оказаться предпочтительнее за счет более полного высвобождения присутствующего в проверяемом препарате эндотоксина.
Безусловно, первые результаты недостаточны для того, чтобы сделать весомые выводы и рекомендации. Скорее стали понятны направления, в которых можно развивать дальнейшие исследования. Так для стадии обработки ферментом стоит подобрать наиболее оптимальные отношения объемов препарат/фермент и активность гиалуронидазы. Также стоит внимательно отнестись к подбору препарата гиалуронидазы как с точки зрения ее активности, так и по чистоте по бактериальным эндотоксинам. В целом, если решение данных вопросов провести удачно, то можно подготовить очень неплохую методику проверки целой группы медицинских изделий, которые с каждым годом набирают все большую популярность.
Список использованной литературы.
1. Lapcik L. Jr., Lapcik L., DeSmedt S. et al. Hyaluronan: preparation, structure, properties and applications // Chem Rev. 1998. Vol. 98. Р. 2663–2684.
2. Применение препаратов гиалуроновой кислоты при коксартрозе / Е.А. Беляева, Т.Л. Кобылкина, М.Г. Перикова, А.Е. Брагин // КЛИНИЧЕСКАЯ МЕДИЦИНА И ФАРМАКОЛОГИЯ. – 2015. – Т. 1, № 4 (4). – С. 48-49. – ISSN 2409-3750.
3. Результаты применения гиалуроновой кислоты в сравнении со стандартной терапией хондропротекторами у пациентов с различной степенью гонартроза / В.И. Кузнецов // МЕДИЦИНСКИЙ СОВЕТ. – 2020. – № 2. – С. 111-120. – ISSN: 2079-701X. eISSN: 2658-5790. DOI: 10.21518/2079-701X-2020-2-111-120
4. Гиалуроновая кислота: применение в офтальмологии и терапии синдрома «сухого глаза» / Е.А. Егоров // РМЖ. Клиническая Офтальмология. 2013 – Т. 14, № 2. – С. 71-74. – ISSN 2225-2282
5. Шептулин В. А. О применении инъекционных имплантатов на основе гелей гиалуроновой кислоты в окулопластике / В. А. Шептулин, Я. О. Груша // Современные технологии в офтальмологии. – 2020. – № 4(35). – С. 312-313. – DOI 10.25276/2312-4911-2020-4-312-313. – EDN SVQPDZ. DOI: 10.25276/2312-4911-2020-4-312-313
6. Опыт применения высокомолекулярной гиалуроновой кислоты в лечении хронического генерализованного пародонтита / И.А. Гатило, Т.Л. Кобылкина, М.Г. Перикова, А.Е. Брагин // СТОМАТОЛОГИЯ ДЛЯ ВСЕХ. – 2021. – № 2 (95). – С. 33-37. – ISSN 1999-172X. – eISSN: 2408-9753. DOI: 10.35556/idr-2021-2(95)33-37
7. Применение гиалуроновой кислоты в комплексном лечении заболеваний пародонта / Л.Ю. Орехова, Е.С. Лобода, Н.А. Яманидзе, Н. Бусарова // ЦИФРОВАЯ СТОМАТОЛОГИЯ. – 2019. – Т. 11, № 2. – С. 15-20.
8. Опыт применения гиалуроновой кислоты в профилактике спаечного процесса / А.Н. Коваленко, И.А. Маркин, Е.А. Винокурова // ВОПРОСЫ НАУКИ И ПРАКТИКИ - 2018: 1 СЕССИЯ. – 2018. – Сборник статей III Международной научной конференции. – С. 234-237.

 Вариант для печати
Вариант для печати