Оценка эффективности процедуры депирогенизации качественным и количественным методами проведения ЛАЛ-теста
21.04.2023
Депирогенизацией называют процедуру устранения или разрушения пирогенов, наиболее активными из которых являются эндотоксины грамотрицательных бактерий. Депирогенизации могут подвергаться самые разные объекты.
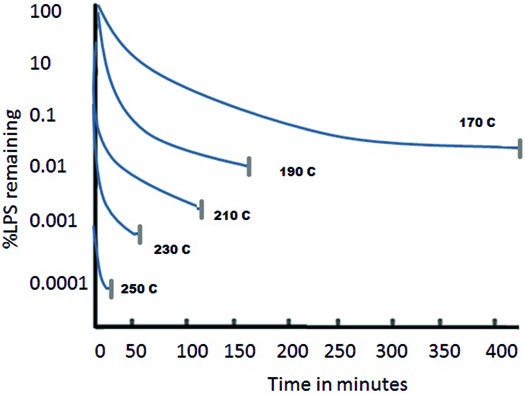
Для депирогенизации медицинских изделий, контейнеров, используемых для первичной упаковки лекарственных средств – ампул, флаконов и пр. применяют термическую депирогенизацию, которая является наиболее простым и надежным способом удаления эндотоксинов. Такая сухожаровая обработка при температуре 250°С в течение 30 минут приводит к практически полной инактивации эндотоксинов [1]. Этот режим упомянут во всех фармакопеях [2,3]. Ранее приемлемым режимом депирогенизации считался нагрев при температуре 180°С в течение трех часов. В процессе изучения динамики термической депирогенизации было показано, что добиться разрушения молекул эндотоксина можно при температурах выше 180°С. При температуре 190°С разрушение эндотоксинов происходит за 65,4 минут, и достаточно всего 1,5 минуты для разрушения эндотоксинов при температуре 250°С. В тоже время при температурах ниже 180°С добиться значительного снижения концентрации эндотоксинов даже за счет увеличения времени экспозиции невозможно [1].
|
| Кривые зависимости скорости разрушения ЛПС от температуры [1] |
Процесс термической депирогенизации применим только к объектам, выдерживающим такую жесткую обработку. Актуальным этот процесс является для обработки стеклянной посуды, используемой для упаковки лекарственных средств или для проведения ЛАЛ-теста. Надо отметить, что процедура термической депирогенизации фактически означает и стерилизацию образцов, причем обратное утверждение неверно. Термическая (сухожаровая или паровая) стерилизация не всегда обеспечивает депирогенизацию обрабатываемых образцов.
Оценки результативности депирогенизации, документы, регламентирующие это действие
Депирогенизация как средство подготовки посуды, используемой для проведения ЛАЛ-теста, упоминается в статье «Бактериальные эндотоксины» [2]. В отечественной фармакопее депирогенизация упоминается также в ОФС.1.1.0016.18 «Стерилизация» [4]. В этой статье в разделе «Стерилизация горячим воздухом» упоминаются режимы 220°С, которые применяют для стерилизации и депирогенизации стеклянной упаковки. Указывается, что должно быть уменьшение на три порядка количества «термостойких эндотоксинов». По сути, это указание на критерии приемлемости процесса – уменьшение на 3 логарифма и указание на необходимость использования специальных препаратов – индикаторов эндотоксина, который назван «термостойкий эндотоксин», что является не очень правильной трансляцией термина «Индикатор эндотоксина».
Индикаторы эндотоксина
Для оценки эффективности процедуры депирогенизации обычно используют специально предназначенные для этой цели препараты эндотоксина. Такие препараты эндотоксина должны отвечать определенным требованиям, наиболее значимые из которых:
1. Содержание эндотоксина во флаконах должно быть достаточно высоким – более 1000 ЕЭ/флакон. Иначе невозможно будет продемонстрировать желаемую степень снижения концентрации эндотоксинов после депирогенизации.
2. Контрольный стандарт эндотоксина должен быть лиофильно высушен и не должен содержать наполнителей, так как препараты КСЭ с наполнителями менее устойчивы при нагревании, следовательно, можно получить недостоверные результаты.
Перечисленным требованиям отвечают не все препараты КСЭ, используемые при проведении ЛАЛ-теста, поэтому гораздо удобнее использовать препараты эндотоксина, созданные специально для проверки депирогенизации. Такие препараты (индикаторы эндотоксина) содержат от нескольких тысяч до сотен тысяч единиц эндотоксина во флаконе [5,6,7].
Прямая и непрямая оценка результативности депирогенизации
Существует два метода оценки эффективности процедуры депирогенизации, соответственно, выпускается и два типа препаратов индикаторов эндотоксинов.
Прямой метод оценки процесса депирогенизации является наиболее простым. Флаконы с КСЭ помещаются в валидируемый сухожаровой шкаф, несколько флаконов оставляют в качестве контроля. По окончании цикла депирогенизации проверяется остаточное содержание эндотоксина во флаконах, подвергнутых обработке, и в контрольных флаконах [8].
Непрямой метод предполагает создание модельного загрязнения флаконов, ампул и т.д. с помощью раствора КСЭ. Затем эти изделия проходят цикл депирогенизации, по окончании которого проверяется остаточное содержание эндотоксинов, это значение сравнивается с содержанием эндотоксинов в контрольных изделиях.
Прямой способ оценки сухожаровой депирогенизации
При проведении валидации сухожаровых шкафов проще всего использовать наборы индикаторов эндотоксинов, предназначенные для проведения валидации прямым методом. Флаконы индикаторов эндотоксина подвергают депирогенизации. Несколько флаконов оставляют необработанными и используют в качестве контроля [8].

В обработанных и необработанных флаконах определяют концентрацию (содержание) эндотоксинов. Полученное значение концентрации в обработанных флаконах сравнивают с содержанием эндотоксинов в необработанных (контрольных) флаконах. Депирогенизация считается эффективной в том случае, если она приводит к снижению концентрации эндотоксинов как минимум в 1000 раз (3 log).
Практическая оценка гель-тромб тестом
Мы на собственном производстве применили концепцию проверки прямым методом и так получилось, что оценку концентрации эндотоксинов мы провели двумя разными методами. Сначала по самой простой схеме оценили степень снижения с помощью гель-тромб теста. Решили использовать только качественный гель-тромб тест, сведя задачу проверки к минимуму – надо показать, что разница концентраций до и после депирогенизации составляет не менее 3 порядков.
Использовали индикаторы эндотоксинов производства Charles River Endosafe кат. номер EVV2K, с заявленной активностью во флаконе не менее 2000 ЕЭ/флакон. Оценку проводили с помощью ЛАЛ-реактива Endosafe KTA с чувствительностью 0,03 ЕЭ/мл. Флаконы с индикаторами эндотоксина (контрольные и обработанные) разводили 1 мл воды для ЛАЛ-теста.
Подготовка контрольных флаконов (не прошедших депирогенизацию). Содержание эндотоксина во флаконе после разведения 1 мл воды должно быть около 2000 ЕЭ/мл. Для ЛАЛ-реактива с чувствительностью 0,03 ЕЭ/мл МДР для такого раствора будет равен 64 000. Точная оценка исходной концентрации эндотоксина в данном случае была необязательна. Нам достаточно было показать, что исходная концентрация эндотоксина была высокой. С точки зрения целесообразности достаточно провести проверку контрольного раствора в разведении 1/10 000. В опыт в этом разведении раствор необработанного индикатора эндотоксина должен обязательно дать положительный результат.
Подготовка флаконов, прошедших депирогенизацию. Поскольку при правильно проведенной термической депирогенизации происходит полное разрушение эндотоксинов, проверка полученного во флаконе раствора проводится без его дополнительного разведения. В опыт ставится раствор, полученный в обработанном флаконе с ИЭ после его разведения 1 мл воды для ЛАЛ-теста. Результат должен быть отрицательным.
Количественная оценка результатов качественного гель-тромб теста.
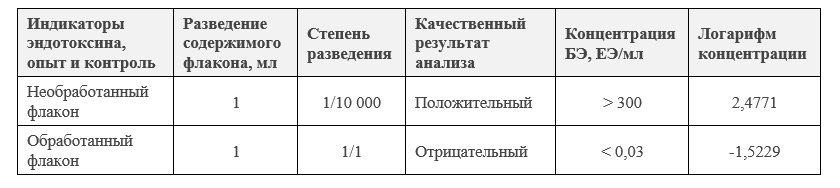
Степень снижения рассчитывается по формуле:
Степень снижения концентрации эндотоксина = log (Конц до обработки, ЕЭ/мл) - log (Конц. После обработки, ЕЭ/мл)
Практический результат:
Степень снижения концентрации эндотоксинов = 2,4771 – (-1,5229) = 4,0
Минимальный уровень снижения должен быть 3 log.
Практически показано снижение не менее чем на 4 log.
Оценка кинетическим турбидиметрическим тестом
Несмотря на удовлетворительные результаты первой части работ по валидации сухожарового шкафа мы решили, что более полным протокол квалификации оборудования будет в том случае, если для оценки степени снижения концентрации эндотоксинов после депирогенизации будет использован количественный метод оценки концентрации индикаторов эндотоксина до и после обработки.
Метод проведения испытания. Для оценки концентрации эндотоксинов был выбран кинетический турбидиметрический метод, метод С. Методика проведения этого анализа хорошо отработана и сам метод верифицирован по всем правилам в нашей Испытательной лаборатории.
Для проведения опытов использовали ЛАЛ-реактив Endosafe KTA 2, калибровочную кривую строили в диапазоне от 0,005 ЕЭ/мл до 5 ЕЭ/мл. Флаконы с индикаторами эндотоксина (контрольные и обработанные), также как и для гель-тромб теста разводили 1 мл воды для ЛАЛ-теста.
Подготовка контрольных флаконов (не прошедших депирогенизацию). Учитывая ожидаемую концентрацию эндотоксина, около 2000 ЕЭ/мл, готовили разведение исходного раствора в 1000 раз. Примерное содержание эндотоксинов в таком растворе должно быть около 2 ЕЭ/мл, такая концентрация будет определяться в калибровочной кривой с диапазоном 0,005 - 5 ЕЭ/мл. В отличие от первого варианта с гель-тромб тестом точная оценка исходной концентрации эндотоксина в данном случае была необходима. Для большей точности использовали не один, а два контрольных флакона, это дало возможность оценить среднее значение концентрации в необработанных флаконах с учетом допустимого разброса результатов.
Подготовка флаконов, прошедших депирогенизацию. Также как и в перовом варианте в обработанных флаконах не ожидается никакой эндотоксиновой активности, поэтому все обработанные флаконы проверяли без разведения. Количество обработанных флаконов в нашем опыте было равно девяти. Оценка содержания эндотоксинов проводилась индивидуально для каждого флакона. Затем данные, полученные по всем девяти флаконам, усреднялись также как и данные для необработанных флаконов.
Количественная оценка результатов кинетического турбидиметрического теста
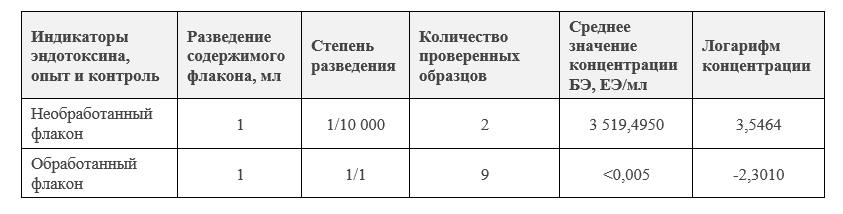
Степень снижения рассчитывается по формуле:
Степень снижения концентрации эндотоксина = log (Конц до обработки, ЕЭ/мл) - log (Конц. После обработки, ЕЭ/мл)
Практический результат:
Степень снижения концентрации эндотоксинов = 3,5464 – (-2,3010) = 5,8475
Практически показано снижение равное 5,85 log.
Протокол квалификации и его оформление.
В конечном счете при оформлении протокола квалификации было решено использовать результаты, полученные во втором цикле опытов, в котором были получены результаты количественного определения активности индикаторов эндотоксина до и после процедуры депирогенизации. Количественные результаты более соответствуют общему складу протокола квалификации, в котором используются такие понятия как критерии достоверности, прецизионность, правильность, статистические алгоритмы оценки концентрации. В таком протоколе желательно использовать и результаты в виде цифровых значений активности, а не качественные понятия больше/меньше.
Ценность количественной оценки
В первой части наших исследований мы показали, что, используя ограниченные возможности качественного анализа, в принципе можно получить данные, подтверждающие достижения эффективного порога депирогенизации в 3 log снижения активности препарата индикатора эндотоксина. Вместе с тем более полную оценку результатам этого процесса дает количественная оценка активности эндотоксина до и после депирогенизации. Результаты получаются более подробными и более убедительными. Такие результаты легче включаются в протоколы квалификации (валидации), предполагающие статистическую обработку и оценку результатов испытания. Не случайно во всех инструкциях на индикаторы эндотоксина подчеркивается, что предпочтительнее проводить количественную оценку содержания эндотоксина до и после обработки кинетическими методами.
Оценочные испытания, проводимые в лаборатории НПО «ЛАЛ-Центр».
Испытательная лаборатория ООО «НПО «ЛАЛ-Центр» разработала оценочную методику квалификации процедуры термической депирогенизации и предлагает проведение исследований индикаторов эндотоксина после процедуры термической депирогенизации в сухожаровых шкафах или стерилизационных туннелях.
Мы предлагаем тем, кому необходима количественная оценка результатов термической обработки, проведение таких исследований на базе нашей лаборатории. Результаты работы могут быть оформлены в виде оценочного протокола квалификации эксплуатации (Performance Qualification) по принятому в лаборатории алгоритму оформления валидационных документов.
1. Tsuji K., Lewis A.R. // Dry-heat destructijn of lipopolysaccaride: Mathematical approach to process evaluation. Appl. Environ. Microbiol. 1978., Vol. 36., No. 5., P. 715-719.
2. ГФ ХIV. ОФС.1.2.4.0006.15 «Бактериальные эндотоксины».
3. <85> Bacterial Endotoxins Test. United States Pharmacopeial Convention, Rockville, MD.
4. ГФ XV. ОФС.1.1.0016.18 «Стерилизация».
5. LAL Users’ Group. 1989. Preparation and Use of Endotoxin Indicators for Depyrogenation Process Studies. J Parent Sci Tech. 43(3): 109-112.
6. 〈1228.5〉 Endotoxin Indicators for depyrogenaton. United States Pharmacopeial Convention, Rockville, MD.
7. Endotoxin challenges in depyrogenation. LAL Update 1990, Vol. 8, No.1.
8. Использование индикаторов эндотоксина для валидации термической депирогенизации // Технический бюллетень No.6., 2019 ООО «НПО «ЛАЛ-Центр».

 Вариант для печати
Вариант для печати